เคมี
ของแข็งผลึก นั้นเป็นที่ตั้งของโมเลกุลตอบสนองต่อคำสั่งที่แน่นอนที่ทำซ้ำทั่วทั้งโครงสร้าง ของแข็งผลึกบางชนิดเป็นผลึกเพชรและเกลือ สถานะของแข็งเป็นหนึ่งซึ่งโมเลกุลของวัสดุอยู่ใกล้กัน วิธีการที่พวกเขาจะรองรับก่อให้เกิดประเภทของโครงสร้างที่แตกต่างกัน ประเภทของโครงสร้างผลึก วิธีการจัดเรียงโครงสร้างผลึกจะได้รับจากเครือข่าย Bravais: P, C, I และ F นอกจากนี้ยังมีระบบผลึกซึ่งสามารถ: - Triclinics - Monoclinics - Orthorhombic - Tetragonal - Rhombohedral - หกเหลี่ยม - ลูกบาศก์ ตัวอย่างหลัก 10 ประการของของแข็งผลึก เกลือ 1- โต๊ะ โซเดียมคลอไรด์เป็นตัวอย่างที่ดีที่สุดของของแข็งผลึกและมีโครงสร้างผลึกของ FCC กับระบ
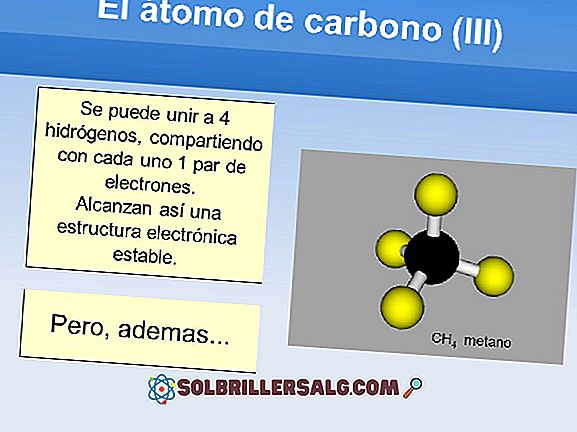
ปริมาณของ อิเล็กตรอนวาเลนซ์ที่คาร์บอนมี อยู่ 4 อิเล็กตรอนของวาเลนซ์เป็นอนุภาคที่มีประจุลบและเป็นส่วนหนึ่งของโครงสร้างภายนอกของอะตอมขององค์ประกอบต่าง ๆ ของตารางธาตุ อิเล็กตรอนวาเลนซ์คืออิเล็กตรอนที่อยู่ในชั้นนอกสุดของอะตอมและมีหน้าที่รับผิดชอบในการปฏิสัมพันธ์ของแต่ละองค์ประกอบกับผู้อื่นเพื่อสร้างพันธะและความมั่นคงและความแข็งแรงของสิ่งเหล่านี้ การเปรียบเทียบเพื่อทำความเข้าใจวิธีการเชื่อมโยงเกิดขึ้นคือการคิดว่าวาเลนซ์อิเล็กตรอนเป็นมือข้างหนึ่งที่คว้าอีกอัน ชั้นวาเลนต์สุดสุดจะต้องถูกเติมเต็มเพื่อให้มีเสถียรภาพอย่างสมบูรณ์และนั่นคือวิธีที่จะเกิดพันธะขึ้น อิเล็กตรอนและวาเลนซ์คาร์บอน ตามที่ระบุไว้ข้าง
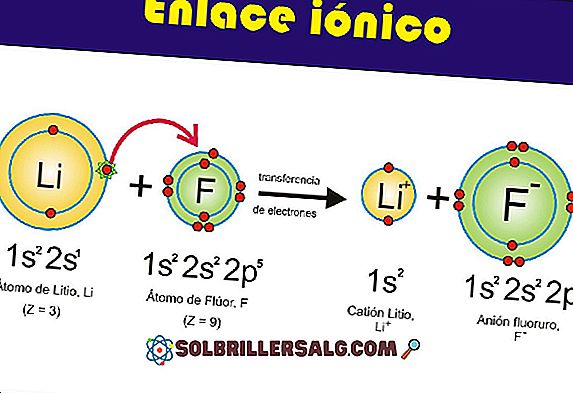
ตัวอย่างของพันธะโควาเลนต์แบบไม่มีขั้ว ได้แก่ คาร์บอนไดออกไซด์อีเทนและไฮโดรเจน พันธะโควาเลนต์เป็นพันธะชนิดหนึ่งที่ก่อตัวขึ้นระหว่างอะตอมเติมชั้นสุดท้ายของความจุและสร้างพันธะที่มีความเสถียรสูง ในพันธะโควาเลนต์มันเป็นสิ่งจำเป็นที่อิเลคโตรเนกาติวีตี้ระหว่างธรรมชาติของอะตอมไม่มากนักเนื่องจากถ้าเกิดเหตุการณ์นี้จะเกิดพันธะไอออนิกขึ้น ด้วยเหตุนี้พันธะโควาเลนต์จึงเกิดขึ้นระหว่างอะตอมกับธรรมชาติที่ไม่ใช่โลหะเนื่องจากโลหะที่ไม่ใช่โลหะจะมีความแตกต่างทางไฟฟ้าขนาดใหญ่อย่างน่าทึ่งและพันธะไอออนิกจะได้รับ ประเภทของพันธะโควาเลนต์ มีการกล่าวกันว่ามีความจำเป็นที่จะต้องไม่มีอิเลคโตรเนกาติตี้ที่สำคัญระหว่างอะตอมหนึ่
องค์ประกอบของของเหลว เป็นสิ่งที่อยู่ในธรรมชาติภายใต้สภาวะอุณหภูมิและความดันปกติไม่มีรูปแบบที่แน่นอน แต่ใช้รูปร่างของภาชนะบรรจุที่มีอยู่ แม้ว่าองค์ประกอบของของเหลวจะไม่มีรูปร่างที่แน่นอน แต่ก็มีคุณสมบัติที่แตกต่างกันซึ่งควรค่าแก่การเน้นเช่นปริมาตรซึ่งเป็นพื้นที่ที่ครอบครองโดยองค์ประกอบนั้น ของเหลวก็มีการเกาะติดกันซึ่งเป็นแรงดึงดูดระหว่างโมเลกุลที่เท่ากัน และการยึดเกาะซึ่งเป็นแรงดึงดูดระหว่างโมเลกุลที่แตกต่างกัน 10 ตัวอย่างหลักขององค์ประกอบของเหลว 1- Bromo (Br) มันเป็นองค์ประกอบสีน้ำตาลแดงที่เป็นของครอบครัวของฮาโลเจน เช่นเดียวกับสิ่งเหล่านี้มันเป็นรูปเกลือและยังทำหน้าที่เป็นตัวออกซิไดซ์ในปฏิกิริย
กระบวนการทางเคมีคือการกระทำใด ๆ ที่ช่วยให้คุณสามารถนำวัสดุและเปลี่ยนเป็นผลิตภัณฑ์ขั้นสุดท้ายที่มีคุณสมบัติแตกต่างกัน โดยทั่วไปกระบวนการทางเคมีสามารถปรับเปลี่ยนคุณสมบัติเงื่อนไขหรือสถานะขององค์ประกอบเพื่อให้สามารถใช้งานได้แตกต่างกัน ในชีวิตประจำวันมีกระบวนการทางเคมีมากมายซึ่งส่วนใหญ่มีความสำคัญในวงจรธรรมชาติและในโลกอุตสาหกรรม เป็นอุตสาหกรรมที่มีการใช้กระบวนการและปฏิกิริยาเคมีเป็นส่วนใหญ่ไม่ว่าจะเพื่อสร้างวัสดุที่ทนต่อหรือมีเงื่อนไขที่เหมาะสมกว่าสำหรับวัตถุประสงค์เฉพาะ ตัวอย่างปฏิกิริยาและกระบวนการทางเคมี กระบวนการทางเคมีบางอย่างเช่นการสังเคราะห์ด้วยแสงเกิดขึ้นตามธรรมชาติในขณะที่กระบวนการอื่น ๆ เ
เคมี มีหน้าที่ศึกษาเรื่ององค์ประกอบองค์ประกอบและโครงสร้างของมันในระดับจุลภาคนั่นคือในระดับอนุภาคที่เล็กที่สุดและความสามารถในการเปลี่ยนแปลงตัวเองโดยการโต้ตอบกันและกับร่างกายอื่น ๆ ซึ่งเป็นสิ่งที่ ซึ่งเขาเรียกว่าปฏิกิริยาเคมี มันเป็นวินัยของวิทยาศาสตร์ธรรมชาติที่ศึกษาอิเลคตรอนโปรตอนและนิวตรอนขององค์ประกอบเรียกว่าอนุภาคอย่างง่ายและอนุภาคคอมโพสิต (อะตอมโมเลกุลและนิวเคลียสอะตอม) ปฏิสัมพันธ์และการเปลี่ยนแปลง การศึกษาวิชาเคมีจากต้นกำเนิด แม้ว่าบางครั้งมันจะไม่ปรากฏชัดเจนเคมีมีอยู่ในทุกองค์ประกอบที่ล้อมรอบเราไม่ว่าจะเป็นสิ่งมีชีวิตหรือวัตถุที่ไม่มีชีวิต ทุกสิ่งที่รู้จักบนโลกของเราและข้างนอกประกอบด้วยอะ
ความ สำคัญของเคมีนั้น อยู่ที่การใช้งานที่หลากหลายในทุกวันนี้ มันถูกใช้ในพื้นที่สำคัญเช่นอาหารหรือยา เคมีหมายถึงวิทยาศาสตร์เชิงทดลองที่ศึกษาคุณสมบัติของสารและรูปแบบเบื้องต้นของสสาร ในทำนองเดียวกันมันศึกษาพลังงานและปฏิสัมพันธ์ระหว่างมันกับสสาร เพราะทุกอย่างประกอบด้วยสสารเคมีจึงเป็นหนึ่งในสาขาที่สำคัญที่สุดของวิทยาศาสตร์ แม้แต่สิ่งมีชีวิตก็ยังมีองค์ประกอบทางเคมีที่มีปฏิสัมพันธ์ซึ่งกันและกัน วิทยาศาสตร์นี้ช่วยให้เราเข้าใจความสัมพันธ์ระหว่างสิ่งมีชีวิตกับโลกรอบตัวพวกเขา ในปัจจุบันเคมีได้ย่อยในสาขาต่างๆที่เกี่ยวข้องกับความรู้ที่แตกต่างกัน ตัวอย่างเช่นชีววิทยาฟิสิกส์และการแพทย์เป็นต้น ความสำคัญของเคมี
เกลือพื้นฐาน คือสิ่งที่อยู่ในโครงสร้างของมันมีไอออนพื้นฐานบางอย่างเช่นไฮดรอกไซด์ (OH) ตัวอย่างบางส่วน ได้แก่ MgCl (OH) (แมกนีเซียมไฮดรอกซิลไรด์), CaNO3 (OH) (แคลเซียม hydroxynitrate) และ Mg (OH) NO3 (แมกนีเซียมแมกนีเซียมไนเตรตพื้นฐาน) เกลือเป็นผลิตภัณฑ์เคมีที่เกิดจากพันธะไอออนิกของไอออนบวก (สารประกอบบวก) และประจุลบ (สารประกอบเชิงลบ) และขึ้นอยู่กับความเข้มของประจุของแต่ละสารประกอบที่เป็นกลางเกลือหรือกรดพื้นฐานสามารถเกิดขึ้นได้ นั่นคือเหตุผลที่เมื่อสหภาพนี้เกิดขึ้นกับประจุลบที่แข็งแกร่งกว่าไอออนบวกความไม่สมดุลเกิดขึ้นในอิเลคโตรเนกาติวีตี้และผลที่ได้คือเกลือพื้นฐาน คุณสมบัติหลักของเกลือพื้นฐาน สูต
อลูมิเนียมโบรไมด์ เป็นสารประกอบที่เกิดจากอะตอมอลูมิเนียมและอะตอมโบรมีนในปริมาณที่แตกต่างกัน มันเกิดขึ้นขึ้นอยู่กับปริมาณของอิเล็กตรอนวาเลนซ์ที่อลูมิเนียมมี เป็นสารประกอบที่ถูกผูกไว้ด้วยโลหะ (อลูมิเนียม) และไม่ใช่โลหะ (โบรมีน) พันธะโควาเลนต์ถูกสร้างขึ้นซึ่งทำให้โครงสร้างมีความเสถียรที่ดีมาก แต่ไม่ถึงพันธะไอออนิก อลูมิเนียมโบรไมด์เป็นสารที่เกิดขึ้นตามปกติในสถานะของแข็งด้วยโครงสร้างผลึก สีของโบรไมด์อลูมิเนียมที่แตกต่างกันจะปรากฏเป็นสีเหลืองอ่อนของเฉดสีที่แตกต่างกันและบางครั้งก็ปรากฏขึ้นโดยไม่มีสี สีขึ้นอยู่กับความสามารถในการสะท้อนแสงที่สารประกอบมีและเปลี่ยนแปลงขึ้นอยู่กับโครงสร้างที่สร้างขึ้นและรู
ตัวอย่างของของแข็งอสัณฐาน คือเทอร์โมพลาสติกโพลีเมอร์, เทอร์โมเซตโพลีเมอร์, อีลาสโตเมอร์, โพลีเมอร์ที่ขยายได้หรือแก้ว Amorphous มาจากภาษากรีกซึ่งคำนำหน้า "a" คือการปฏิเสธและคำ morfo หมายถึงรูปแบบนั่นคือไร้รูปแบบ เมื่อเราพูดถึงของแข็งอสัณฐานเราพูดถึงสถานะของแข็งของสสารที่อนุภาคที่ทำขึ้นไม่มีโครงสร้างที่สั่งซึ่งทำให้ของแข็งเหล่านี้มีรูปร่างไม่แน่นอน หลายครั้งที่ผิดปกติเหล่านี้สามารถเกิดขึ้นได้เนื่องจากลักษณะของอนุภาคหรือถ้าพวกเขาเป็นส่วนผสมของโมเลกุลที่ไม่สามารถซ้อนกันได้อย่างถูกต้อง ตัวอย่างที่แนะนำของของแข็งอสัณฐาน มีตัวอย่างมากมายในธรรมชาติที่จะเข้าใจของแข็งอสัณฐาน อย่างไรก็ตามพวกเขาย
ความ แตกต่างระหว่างของผสมที่ เป็น เนื้อเดียวกันและต่างกัน ขึ้นอยู่กับการมองเห็นของส่วนประกอบความง่ายในการแยกและการอนุรักษ์คุณสมบัติ เป็นที่ทราบกันดีว่าสารผสมนั้นประกอบด้วยสารสองชนิดขึ้นไป แต่มีสารผสมสองชนิดที่สามารถเกิดขึ้นได้จากการผสมเหล่านี้ ในการผสมที่เป็นเนื้อเดียวกันเงื่อนไขและคุณสมบัติของสารประกอบช่วยให้พวกเขาผสมกันจนถึงจุดที่พวกเขาไม่สามารถแยกความแตกต่างจากกันและกันเช่นในกรณีของมายองเนส ในส่วนผสมที่ต่างกันสารประกอบที่ก่อตัวเป็นตัวผลักกันเนื่องจากลักษณะของพันธะของมันเช่นในกรณีของน้ำและน้ำมัน ด้านล่างมีความแตกต่างระหว่างส่วนผสมที่เป็นเนื้อเดียวกันและต่างกัน: ความชัดเจน ในส่วนผสมที่ต่างกันส
การแตกตัวเป็นไอออนเป็นกระบวนการที่อนุภาคหรือองค์ประกอบถูกทิ้งให้มีประจุที่แน่นอนมากบวกหรือลบไม่ว่าจะเกิดจากการขาดหรืออิเล็กตรอนมากเกินไปตามลำดับ ไอออนไนซ์ในสารสามารถทำได้ผ่านกระบวนการทางกายภาพและทางเคมี กระบวนการทางเคมีส่วนใหญ่เป็นปฏิกิริยาที่เกี่ยวข้องกับกรด, พื้นฐาน, สารเป็นกลางและตัวกลางการถ่ายโอนมักจะมีน้ำ กระบวนการทางกายภาพในการแตกตัวเป็นไอออนนั้นขึ้นอยู่กับคลื่นแม่เหล็กไฟฟ้าและความยาวคลื่นที่แตกต่างกันซึ่งสามารถใช้งานได้ ตัวเลือกอื่น ๆ และที่พบมากที่สุดคืออิเล็กโทรไลซิสซึ่งเกี่ยวข้องกับการใช้กระแสไฟฟ้าที่สามารถแยกได้ ตัวอย่างไอออไนซ์ที่แนะนำ 1. แคลเซียมไนไตรด์ (Ca3N2) สารนี้สามารถแยกตัวออ
ตัวอย่างของแอลกอฮอล์ ได้แก่ เอทานอลกลีเซอรอลและแอลกอฮอล์ไอโซโพรพิล แอลกอฮอล์เป็นสารเคมีอินทรีย์ที่มีโมเลกุลไฮดรอกซิลหนึ่งโมเลกุลหรือมากกว่านั้นในโซ่คาร์บอนในรูปแบบอิ่มตัว มีการใช้แอลกอฮอล์ในหลายพื้นที่: จากการบริโภคเครื่องดื่มไปจนถึงตัวทำละลายอุตสาหกรรม แอปพลิเคชั่นนี้มีความหลากหลายมากเนื่องจากมีสิ่งอำนวยความสะดวกในการสังเคราะห์ ประเภทของแอลกอฮอล์ขึ้นอยู่กับโครงสร้างที่โมเลกุลของไฮดรอกไซด์ติดอยู่ดังนั้นพวกมันจึงแตกต่างกันมากและในเวลาเดียวกันก็มีลักษณะบางอย่างร่วมกัน 10 ตัวอย่างหลักของแอลกอฮอล์ 1- เมทานอล เมทานอลเป็นแอลกอฮอล์ชนิดหนึ่งที่เกิดขึ้นจากมีเธน (CH4) แทนที่จะมีไฮโดรเจนเป็นกลุ่มไฮดรอกซิล
โลหะผสม เหล็กเป็น ส่วนผสมที่ เป็นเนื้อเดียวกันซึ่งส่วนใหญ่เป็นเหล็กที่มีการเติมคาร์บอนเข้าไป ของโลหะที่ใช้มากที่สุด, อัลลอยด์ส่วนใหญ่คือ: เหล็ก (Fe), ทองแดง (Cu), โครเมียม (Cr), สังกะสี (Zn), อลูมิเนียม (Al), ไทเทเนียม (Ti), นิกเกิล (Ni), โคบอลต์ (Co) ), แมงกานีส (Mn), ดีบุก (Sn), แมกนีเซียม (Mg), ตะกั่ว (Pb) และโมลิบดีนัม (Mo) โลหะและโลหะผสมของพวกมันถูกจำแนกออกเป็น 2 กลุ่ม: (1) เหล็ก, พวกที่อยู่บนพื้นฐานของเหล็กและ (2) ที่ไม่ใช่เหล็ก, อื่น ๆ ทั้งหมด ลักษณะของโลหะผสมเหล็ก โลหะผสมที่มีคาร์บอนน้อยกว่า 2% (C) ถูกจัดประเภทเป็นเหล็กในขณะที่โลหะที่มีมากกว่า 2% C นั้นเรียกว่าเหล็กหล่อหรือเหล็กหล่อ ในก
ความ สำคัญ หลัก ของตารางธาตุ คือความพึงพอใจต่อความต้องการของนักวิทยาศาสตร์ที่ต้องอธิบายลักษณะของอะตอมเคมีที่ค้นพบโดยจอห์นดัลตัน ทฤษฎีและการสืบสวนดำเนินไปจนถึงขณะนี้กำลังขว้างความคล้ายคลึงกันในมวลอะตอมขององค์ประกอบบางอย่างตามคุณสมบัติของพวกเขา ในปี 1817 Döbereinerรับรองว่ามีความคล้ายคลึงกันดังกล่าวและจัดกลุ่มพวกเขาในสิ่งที่เขาเรียกว่า triads ในปี 1850 มีมากกว่า 20 คณะ ใน 1, 862 Chancourtois บ่งชี้ว่ามีระยะเวลาในองค์ประกอบ. การยืนยันนี้นำไปสู่ว่าในปี ค.ศ. 1864 Chancourtois ใน บริษัท ของ Newlands ได้สร้างกฏที่เรียกว่าอ็อกเทฟขึ้นมา แต่สิ่งนี้ไม่ได้บรรลุความก้าวหน้าใด ๆ หลังจากแคลเซียม ใน 1, 869 Mey
เคมีในชีวิตประจำวัน เป็นเรื่องง่ายที่จะเข้าใจ มันสามารถพบได้ในอาหารที่บริโภคในอากาศที่หายใจในสารเคมีทำความสะอาดและแท้จริงในทุกวัตถุที่อยู่รอบ ๆ มนุษย์ทุกคนทำจากสารเคมีและทุกสิ่งที่อยู่รอบตัวมนุษย์ทำจากสารเคมี ทุกสิ่งที่มนุษย์ได้ยินได้ยินสัมผัสกลิ่นและทดสอบเกี่ยวข้องกับเคมีและสารประกอบอินทรีย์ ประสาทสัมผัสทั้งหมดเกี่ยวข้องกับปฏิกิริยาเคมีและปฏิกิริยา เคมีไม่ จำกัด เฉพาะห้องปฏิบัติการ มันมีอยู่ทั่วโลกและมีอยู่ในทุกด้านของชีวิตประจำวัน โดยพื้นฐานแล้วจะไม่มีอะไรในโลกถ้าไม่มีสารเคมี เคมี 30 ตัวอย่างที่สำคัญในชีวิตประจำวัน 1- กรดอินทรีย์ พวกเขาเป็นสารประกอบเคมีอินทรีย์ที่มีคุณสมบัติเป็นกรด โพรเพนกรดอ
ทฤษฎีการชน เปิดเผยหลักการของ ปฏิกิริยาเคมีทุกครั้งนั้นเกิดขึ้นได้เนื่องจากโมเลกุลอะตอมหรือไอออนของรีเอเจนต์ที่เกี่ยวข้องกับการชนกัน การปะทะกันระหว่างเผ่าพันธุ์จะไม่เหมือนเดิมเสมอไป ขึ้นอยู่กับความเข้มข้นและประเภทของรีเอเจนต์ที่คุณใช้งาน ในระดับที่ความเข้มข้นของรีเอเจนต์เพิ่มขึ้นจำนวนการกระแทกเพิ่มขึ้น ตรงกันข้ามจะเกิดขึ้นหากความเข้มข้นลดลง นี่เป็นเพราะความจริงที่ว่าความเข้มข้นของสารตั้งต้นเพิ่มขึ้นยิ่งจำนวนของอะตอมมากขึ้นและยิ่งมีการชนกันมากขึ้น อย่างไรก็ตามการชนกันทั้งหมดไม่ได้มีประสิทธิภาพและดังนั้นโมเลกุลที่ตอบสนองทั้งหมดจะสร้างผลิตภัณฑ์ หากเป็นกรณีนี้ปฏิกิริยาทั้งหมดระหว่างของเหลวหรือสารที่
ประวัติความเป็นมาของวิชาเคมี มาจากกว่า 750, 000 ปีที่ผ่านมาด้วยการค้นพบของไฟโลหะวิทยาการเล่นแร่แปรธาตุ vitalism องค์ประกอบทางเคมีและการพัฒนาทฤษฎีอะตอม ความรู้เกี่ยวกับอารยธรรมโบราณในการเปลี่ยนสสารการสกัดโลหะและการผลิตโลหะผสมรวมถึงการทำรายละเอียดของแก้วและเซรามิกเป็นความรู้เบื้องต้นเกี่ยวกับเคมี แม้แต่การรักษาผลไม้หมักเพื่อสร้างเหล้าหรือการสกัดพืชสมุนไพรก็มี เคมีทำให้งานของมนุษย์ง่ายขึ้นและปรับปรุงคุณภาพชีวิตมานานหลายศตวรรษ จากยุคก่อนประวัติศาสตร์จนถึงปัจจุบันการศึกษาอย่างเป็นทางการของเคมีได้รับอนุญาตให้ปรับเปลี่ยนความสัมพันธ์ที่มีอยู่ระหว่างธรรมชาติและมนุษย์ การค้นพบหลัก 7 ประการของวิชาเคมีในปร
กลุ่มฟอสเฟต เป็นโมเลกุลที่เกิดขึ้นจากอะตอมฟอสฟอรัสที่ติดกับอะตอมออกซิเจนสี่อะตอม สูตรทางเคมีของมันคือ PO43- อะตอมกลุ่มนี้เรียกว่ากลุ่มฟอสเฟตเมื่อถูกยึดติดกับโมเลกุลที่มีคาร์บอน (โมเลกุลชีวภาพใด ๆ ) สิ่งมีชีวิตทั้งหมดทำจากคาร์บอน กลุ่มฟอสเฟตมีอยู่ในสารพันธุกรรมในโมเลกุลที่มีความสำคัญสำหรับการเผาผลาญของเซลล์ซึ่งเป็นส่วนหนึ่งของเยื่อชีวภาพและระบบนิเวศน้ำจืด เห็นได้ชัดว่ากลุ่มฟอสเฟตมีอยู่ในโครงสร้างที่สำคัญของสิ่งมีชีวิต อิเล็กตรอนที่ใช้ร่วมกันระหว่างอะตอมออกซิเจนทั้งสี่กับอะตอมคาร์บอนสามารถเก็บพลังงานได้จำนวนมาก ความสามารถนี้มีความสำคัญสำหรับบทบาทของพวกเขาในเซลล์ หน้าที่หลัก 6 ประการของกลุ่มฟอสเฟต
ความสามารถในการละลาย คือจำนวนตัวถูกละลายสูงสุดที่สามารถละลายในตัวทำละลายในสมดุลดังนั้นจึงเป็นวิธีการแก้ปัญหาอิ่มตัว สารที่ละลายได้คือสิ่งที่เมื่อสัมผัสกับของเหลวอื่นให้ละลายและก่อตัวเป็นสารละลาย สารที่ละลายคือตัวถูกละลายและสารที่ละลายคือตัวทำละลาย การแก้ปัญหาคือส่วนผสมระหว่างตัวถูกละลายและตัวทำละลาย ตัวถูกละลายและตัวทำละลายสามารถพบได้ในสถานะของเหลวของแข็งและก๊าซ วัสดุหรือสารแลกเปลี่ยนอิเล็กตรอนเหล่านี้เมื่อสัมผัสในสัดส่วนที่เหมาะสม ส่งผลให้เกิดการก่อตัวของสารประกอบใหม่ ตัวทำละลายสากลคือน้ำ อย่างไรก็ตามวัสดุหรือสารบางชนิดไม่สามารถละลายได้ 20 ตัวอย่างความสามารถในการละลายของวัสดุและสารที่ละลายได้
เกลือไบนารี เป็นสารประกอบทางเคมีที่มีต้นกำเนิดมาจากส่วนผสมของโลหะและไม่ใช่โลหะ ในเกลือแบบไบนารีองค์ประกอบที่ไม่ใช่โลหะจะใช้เวเลนซ์ที่ต่ำกว่าเสมอ เกลือไบนารีรู้จักกันในชื่อเกลือเป็นกลาง พวกมันคืออนุพันธ์ของไฮดราไซด์นั่นคือการรวมกันของอะตอมไฮโดรเจน (H) กับอะตอมแอมฟิฟิลิก (ซัลเฟอร์ซีลีเนียมเทลลูโลสเทลูเนียมและพอโลเนียม) หรือฮาโลเจน ในวัสดุประเภทนี้ไฮโดรเจนจะถูกแทนที่ด้วยโลหะ จากนั้นสารประกอบจะถูกสร้างขึ้นโดยมีส่วนร่วมของฮาโลเจนหรือแอมฟิฟิลส์และโลหะ ดังนั้นเกลือแบบไบนารีสามารถเป็นได้หลายประเภท: ไอโอไดด์, แอสเทมท์, ซัลไฟด์, เทลลูไรด์, เซเลไนด์, ฟลูออไรด์, คลอไรด์, โบรไมด์และอื่น ๆ ลักษณะของเกลือไบนา
คาร์บอนอสมมาตร เป็นอะตอมของคาร์บอนที่ติดอยู่กับองค์ประกอบทางเคมีที่แตกต่างกันสี่แบบ ในโครงสร้างนี้อะตอมของคาร์บอนอยู่ตรงกลางเชื่อมโยงองค์ประกอบที่เหลือผ่านเข้าไป โมเลกุลของ bromochloroodomethane เป็นตัวอย่างที่ชัดเจนของคาร์บอนอสมมาตร ในกรณีนี้อะตอมของคาร์บอนเชื่อมโยงกับอะตอมของโบรมีนคลอรีนไอโอดีนและไฮโดรเจนผ่านพันธะเฉพาะ การก่อตัวของประเภทนี้เป็นเรื่องธรรมดามากในสารประกอบอินทรีย์เช่น glyceraldehyde ซึ่งเป็นน้ำตาลธรรมดาที่ได้มาจากกระบวนการสังเคราะห์แสงในพืช ลักษณะของคาร์บอนอสมมาตร คาร์บอนอสมมาตรเป็นคาร์บอนเตตราไฮเดรชั่นที่เชื่อมต่อกับธาตุทั้งสี่ การกำหนดค่านี้คล้ายกับดาวฤกษ์: คาร์บอนอสมมาตรทำหน้
ปฏิกิริยาการสังเคราะห์คือปฏิกิริยาที่สารประกอบสองชนิดขึ้นไปทำปฏิกิริยากับเงื่อนไขบางอย่างเพื่อสร้างผลิตภัณฑ์ใหม่หนึ่งรายการขึ้นไป ในวิธีทั่วไปปฏิกิริยาสามารถแสดงเป็นรูปแบบ: A + B → C ปฏิกิริยาการสังเคราะห์นั้นมีความสำคัญอย่างมากต่อวิทยาศาสตร์เพราะด้วยวิธีการเหล่านี้สามารถทำวัสดุยาและผลิตภัณฑ์ต่าง ๆ ที่เราใช้ในชีวิตประจำวันได้ ตัวอย่างปฏิกิริยาการสังเคราะห์ การผลิตแอมโมเนีย (NH3) โมเลกุลของไนโตรเจนประกอบด้วยสองอะตอมของธาตุนี้ ไฮโดรเจนจะเหมือนกันในวิธีนี้ดังนั้นเมื่อรวมกันในสัดส่วนที่เหมาะสมภายใต้สภาวะความดันและอุณหภูมิที่เหมาะสมแอมโมเนียจะถูกผลิตขึ้นตามปฏิกิริยาต่อไปนี้ N2 + 3H2 → 2NH3 กรดกำมะถั
เคมีของอาหาร เป็นสาขาวิชาเคมีที่ศึกษาสารเคมีที่ทำอาหารองค์ประกอบคุณสมบัติกระบวนการทางเคมีที่เกิดขึ้นในพวกเขาและปฏิกิริยาของสารเหล่านี้ระหว่างพวกเขาและกับองค์ประกอบทางชีวภาพอื่น ๆ ของอาหาร . วินัยนี้ยังรวมถึงแง่มุมที่เกี่ยวข้องกับพฤติกรรมของสารเหล่านี้ในระหว่างการเก็บรักษาการแปรรูปการปรุงอาหารและแม้กระทั่งในปากและในระหว่างการย่อยอาหาร เคมีของอาหารเป็นส่วนหนึ่งของวินัยที่กว้างขึ้นเช่นวิทยาศาสตร์การอาหารซึ่งเกี่ยวข้องกับชีววิทยาจุลชีววิทยาและวิศวกรรมอาหาร ในแง่มุมพื้นฐานที่สุดเคมีพื้นฐานของอาหารเกี่ยวข้องกับส่วนประกอบหลักในพวกเขาเช่นน้ำคาร์โบไฮเดรตไขมัน
ระยะเวลาทางเคมี หรือระยะเวลาของคุณสมบัติทางเคมีเป็นรูปแบบปกติกำเริบและคาดการณ์ได้ในคุณสมบัติทางเคมีขององค์ประกอบเมื่อจำนวนอะตอมเพิ่มขึ้น ด้วยวิธีนี้ช่วงเวลาทางเคมีเป็นพื้นฐานของการจำแนกองค์ประกอบทางเคมีทั้งหมดตามหมายเลขอะตอมและคุณสมบัติทางเคมีของพวกเขา การแสดงภาพของช่วงเวลาทางเคมีเรียกว่าตารางธาตุตารางMendeleïevหรือการจำแนกธาตุเป็นระยะ สิ่งนี้แสดงองค์ประกอบทางเคมีทั้งหมดเรียงตามลำดับหมายเลขอะตอมที่เพิ่มขึ้นและจัดระเบียบตามการกำหนดค่าทางอิเล็กทรอนิกส์ โครงสร้างของมันสะท้อนให้เห็นถึงความจริงที่ว่าคุณสมบัติขององค์ประกอบทางเคมีเป็นฟังก์ชันตามระยะเวลาของเลขอะตอม ช่วงเวลานี้มีประโยชน์มากเพราะอนุญาตให
ความเร็วของปฏิกิริยาเคมีคือความเร็วที่การเปลี่ยนแปลงของสารที่เรียกว่ารีเอเจนต์เกิดขึ้นในสารอื่น ๆ ที่เรียกว่าผลิตภัณฑ์ ปัจจัยที่มีผลต่อความเร็วอาจมีหลายประการ ธรรมชาติของรีเอเจนต์ขนาดอนุภาคสถานะทางกายภาพของสาร ... รีเอเจนต์อาจเป็นอะตอมหรือโมเลกุลที่ชนกันหรือชนกันทำให้เกิดรอยแตกในการเชื่อมโยงระหว่างกัน หลังจากการแบ่งลิงค์ใหม่จะถูกสร้างขึ้นและผลิตภัณฑ์จะเกิดขึ้น หากรีเอเจนต์อย่างน้อยหนึ่งตัวถูกใช้หมดในปฏิกิริยาโดยการสร้างผลิตภัณฑ์โดยสมบูรณ์ปฏิกิริยาจะถูกทำให้สมบูรณ์และมุ่งไปในทิศทางเดียวเท่านั้น ในบางกรณีผลิตภัณฑ์ที่เกิดขึ้นอีกครั้งชนกันอีกครั้งและทำลายลิงก์ของพวกเขาเพื่อจัดระเบียบใหม่และกลายเป็น
สารรีดิวซ์ เป็นสารที่ตอบสนองการทำงานของการลดสารออกซิไดซ์ในปฏิกิริยาการลดออกไซด์ ตัวแทนที่ลดลงเป็นผู้บริจาคอิเล็กตรอนตามธรรมชาติโดยทั่วไปแล้วสารที่อยู่ในระดับต่ำสุดของการเกิดออกซิเดชันและมีอิเล็กตรอนจำนวนมาก มีปฏิกิริยาทางเคมีที่สถานะออกซิเดชันของอะตอมแตกต่างกันไป ปฏิกิริยาเหล่านี้เกี่ยวข้องกับกระบวนการลดและกระบวนการออกซิเดชั่นเสริม ในปฏิกิริยาเหล่านี้อิเล็กตรอนหนึ่งตัวหรือมากกว่าของโมเลกุลอะตอมหรือไอออนจะถูกถ่ายโอนไปยังโมเลกุลอะตอมหรือไอออนอื่น สิ่งนี้เกี่ยวข้องกับการผลิตปฏิกิริยาการลดออกไซด์ ในระหว่างกระบวนการลดออกไซด์องค์ประกอบหรือสารประกอบที่สูญเสีย (หรือบริจาค) อิเล็กตรอน (หรืออิเล็กตรอน) เ
สารออกซิไดซ์ เป็นสารเคมีที่มีความสามารถในการลบอิเล็กตรอนออกจากสารอื่น (สารรีดิวซ์) ที่บริจาคหรือสูญเสียพวกมัน หรือที่เรียกว่าตัวออกซิไดซ์คือองค์ประกอบหรือสารประกอบที่ส่งผ่านอิเลคโตรเนกาติตี้อะตอมไปยังสารอื่น เมื่อมีการศึกษาปฏิกิริยาทางเคมีสารทั้งหมดที่เข้ามาแทรกแซงและกระบวนการที่เกิดขึ้นในพวกเขาจะต้องนำมาพิจารณา สิ่งที่สำคัญที่สุดคือปฏิกิริยาการลดออกซิเดชั่นหรือที่เรียกว่ารีดอกซ์ซึ่งเกี่ยวข้องกับการถ่ายโอนหรือถ่ายโอนอิเล็กตรอนระหว่างสปีชีส์เคมีสองชนิดหรือมากกว่า ในปฏิกิริยาเหล่านี้มีปฏิกิริยาสองอย่างคือสารรีดิวซ์และสารออกซิไดซ์ สารออกซิไดซ์บางตัวที่สามารถสังเกตได้บ่อยครั้งคือออกซิเจนไฮโดรเจนโอโ
การ ไฮบริไดเซชันของคาร์บอน เกี่ยวข้องกับการรวมกันของสองอะตอมออร์บิทัลบริสุทธิ์เพื่อสร้างวงโคจรระดับโมเลกุล "ไฮบริด" ใหม่ที่มีลักษณะเฉพาะ ความคิดเกี่ยวกับการโคจรของอะตอมให้คำอธิบายที่ดีกว่าแนวคิดวงโคจรก่อนหน้านี้เพื่อสร้างการประมาณว่ามีความน่าจะเป็นมากในการค้นหาอิเล็กตรอนในอะตอม อีกวิธีหนึ่งการโคจรของอะตอมเป็นตัวแทนของกลศาสตร์ควอนตัมเพื่อให้ความคิดเกี่ยวกับตำแหน่งของอิเล็กตรอนหรือคู่ของอิเล็กตรอนในบางพื้นที่ภายในอะตอมซึ่งแต่ละวงถูกกำหนดตามค่าของตัวเลข ควอนตัม ตัวเลขควอนตัมอธิบายสถานะของระบบ (เช่นเดียวกับอิเล็กตรอนในอะตอม) ในช่วงเวลาหนึ่งโดยพลังงานที่เป็นของอิเล็กตรอน (n) โมเมนตัมเชิงมุ
ความพรุนของสารเคมี คือความสามารถของวัสดุบางชนิดในการดูดซับหรือปล่อยให้สารบางอย่างในสถานะของเหลวหรือก๊าซผ่านช่องว่างที่มีอยู่ในโครงสร้างของมัน เมื่อพูดถึงความพรุนส่วนของ "ช่องว่าง" หรือช่องว่างในวัสดุที่กำหนดจะถูกอธิบาย มันถูกแทนด้วยส่วนปริมาณของฟันผุเหล่านี้หารด้วยปริมาณของวัสดุทั้งหมดที่ศึกษา ขนาดหรือค่าตัวเลขที่เป็นผลมาจากพารามิเตอร์นี้สามารถแสดงได้สองวิธี: ค่าระหว่าง 0 ถึง 1 หรือเปอร์เซ็นต์ (ค่าระหว่าง 0 ถึง 100%) เพื่ออธิบายว่าวัสดุมีพื้นที่ว่างเท่าใด แม้จะถูกนำมาใช้หลายอย่างในสาขาต่าง ๆ ของวิทยาศาสตร์บริสุทธิ์, การนำไปใช้, วัสดุ, ในหมู่คนอื่น ๆ, หน้าที่หลักของความพรุนทางเคมีนั้นเ